
一、政策战略定位
1.产业链强链工程:
▸ 精准卡位CDMO/CRO等产业关键节点
▸ 强制要求通过NMPA/GMP认证
2.创新能级跃升:
重点扶持方向:
▶ 填补重庆空白的首台设备。
▶ 绿色制药技术。
二、申报条件精准拆解
▎核心赛道定义:
✅ 研发平台类:GLP实验室/药物晶型研究系统(投资≥2000万)
✅ 生产建设类:
» 器械产线:智能吻合器等(投资≥500万)
» 药品产线:细胞治疗制剂等(投资≥3000万)
▎创新门槛要求:
⚠️ 必须符合以下任一特征:
» 重庆首次引进的研发技术平台(需科技查新报告)
» 实现进口替代的核心设备(需提供竞品对标分析)
» 绿色制药工艺(单位产品能耗下降≥30%)
三、奖补标准详解
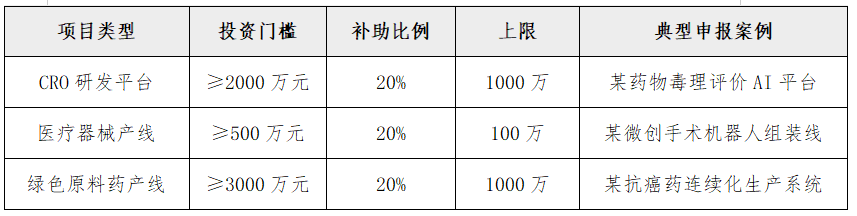
四、申报材料攻坚指南
1.专项审计核心点:
▶ 设备分类:需拆分研发设备/生产设备/检测设备占比
▶ 软件投入:与研发活动的直接关联性证明(如CFDA认证系统)
2.绩效举证策略:
▶ 技术突破类:发明专利授权书+科技成果登记证书
▶ 替代进口类:海关进口数据对比+客户采购证明
3.典型材料缺陷:
▶ 设备照片未标注唯一性标识(与采购合同对应)
▶ 未提供实验室CNAS认证或车间GMP符合性检查报告
五、申报全流程导航
1.项目合规预审
▶ 核查项目是否符合政策支持方向,重点验证:
▶ 是否属于药物筛选/安全评价/医疗器械研发等指定领域
▶ 是否达到器械类500万/药品类3000万投资门槛
2.创新性资质审查
▶ 若属于填补市内空白项目:需提交《重庆市首台(套)重大技术装备认定书》或省级以上科技查新报告
▶ 若不属于:需补充申报期内获得的发明专利(至少2项)或PCT国际专利
3.设备投资专项审计
由具备审计资质的机构出具报告,重点验证:
▶ 设备与研发/生产活动的直接关联性(如HPLC仪器用于药物分析)
▶ 软件费用合理性(需提供功能模块与GLP/GMP认证对应关系)
4.现场核查重点:
▶ 设备实际运行状态(需开机演示)
▶ 与申报产能匹配性(如冻干机数量与年产百万支制剂的关系)
六、专业服务优势
✅ 创新性证明体系:
▸ 药智网全球药品专利检索报告
▸ 国家药监局医疗器械优先审批通道申请
✅ 设备关联性强化:
» 与治疗指南/药典标准的适配性分析
» 进口设备替代效益测算模型
✅ 风险防控机制:
▶ 设备进场时间与投资进度校验系统
▶ 加急申报服务(重大疾病领域项目加急申报)

-
2026-03-21
-
2026-03-21
-
2026-03-21







